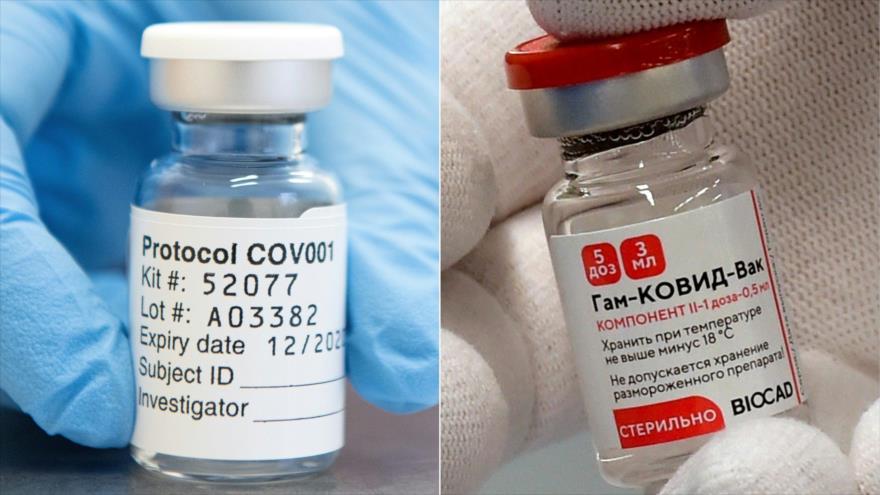
“Anunciamos un programa de ensayos clínicos para evaluar la seguridad y la inmunogenicidad de la combinación de AZD1222, desarrollada por AstraZeneca y la Universidad de Oxford, y Sputnik V”, vacuna rusa desarrollada por el Instituto de Investigación de Epidemiología y Microbiología Gamaleya, ha informado el laboratorio británico mediante un comunicado publicado este viernes.
El texto ha agregado que las combinaciones de las diferentes vacunas contra la COVID-19 pueden ser una etapa importante para crear una mayor protección, explicando que al unir dos investigaciones se puede lograr una “mejor respuesta inmunitaria”, agregando que los ensayos se realizarán en individuos mayores de 18 años.
“Tanto AZD1222 como la Sputnik V son vacunas de vectores adenovirales que contienen material genético de la proteína espiga del virus SARS-Cov-2. El adenovirus en sí no puede replicarse, por lo que solo puede actuar como portador de material genético”, se lee en el texto.
Los adenovirus son virus que causan resfríos comunes que son modificados genéticamente para que no se repliquen en el organismo. Lo que se hace es “insertar” la parte de la proteína espiga en este adenovirus y, cuando éste ingresa al organismo, el sistema inmune detecta la proteína y genera su respuesta.
Por su parte, el fondo soberano ruso, que participa en el desarrollo de la vacuna contra el coronavirus mediante un comunicado ha indicado que que había propuesto a AstraZeneca el uso de los dos componentes de la vacuna Sputnik V, “AstraZeneca aceptó la propuesta (...) de usar uno de los dos vectores de la vacuna Sputnik V en los ensayos clínicos suplementarios de su propia vacuna, que comenzarán antes de finales de año”, ha detallado.
Rusia dijo el pasado 11 de noviembre que Sputnik V alcanzó un 92 % de efectividad en las primeras pruebas de la fase tres, sin registrar “eventos adversos inesperados”.
shz/lvs/mjs